RV的囊膜糖蛋白(glycoprotein,G)是其逆行跨突触所必需的蛋白,G蛋白缺失的RV(RV-ΔG)会丧失跨突触能力,但其复制及转录不受影响(可持续高丰度表达外源基因),因此,RV-ΔG携带报告基因后,可逆向高亮度标记神经元精细形态。
CVS-N2c病毒株具有更低的神经毒性以及更强的跨突触突触传递能力,其G蛋白缺失的RV(RV-N2C(G)-ΔG)能在更低的滴度达到与第一代RV-ΔG相同甚至更好的逆向标记效果,且神经毒性更低。
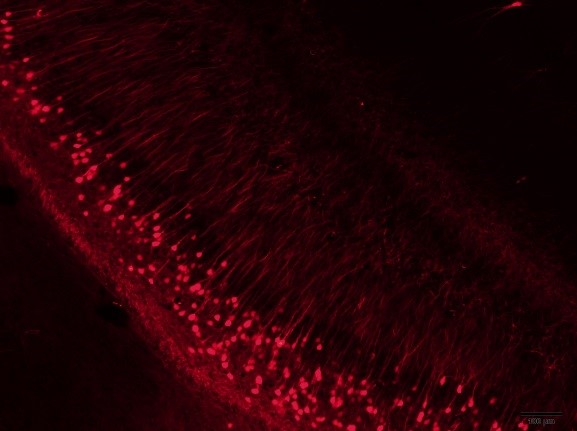
图3 RV-N2C(G)-ΔG-mCherry(枢密科技测试)
利用重组的禽类肉瘤病毒(Aviansarcoma-leukosisvirus,ASLV)的外膜蛋白(EnvA)融合蛋白包装RV形成的病毒粒子,可特异性识别EnvA的受体TVA(TVA只存在于禽类细胞中,在哺乳动物神经元中无表达)介导病毒特异性地感染细胞。利用Cre转基因鼠结合Cre-LoxP控制表达TVA及G蛋白的AAV辅助病毒,可实现只在特定区域特异类型神经元中表达TVA及G蛋白,从而利用RV-EnvA-ΔG实现对特异类型神经元的逆向跨单级突触标记(如图3)。在此基础上,使RV-EnvA-ΔG带上ChR2及GCaMP等基因,可实现对特异类型神经元的直接输出网络进行功能操纵及活动监测。
图4 RV-EnvA-ΔG实现神经元的逆向跨单级突触标记(Callaway et al.,The Journal of neuroscience:the official journal of the Society for Neuroscience, 2015)
1、特定区域特异类型神经元的全脑单级输入网络标记。
2、两个区域特异类型神经元跨单级输入网络标记。
3、三级连接网络的跨单突触标记。
首先将AAV-EF1α-DIO-GFP-TVA与AAV-EF1α-DIO-RVG按照特定比例混合,然后向在特异神经元中表达Cre的转基因小鼠目标脑区立体定位注射AAV混合病毒。待AAV病毒充分表达两周以上,即可在同一区域立体定位注射RV-EnvA-ΔG-dsRed,RV注射后一周,可对动物心脏灌注,利用4% PFA固定后取出脑组织制备样本观察标记结果。
1、我们提供的AAV目前均为2/9型或5型,病毒滴度均约为2X10E12 v.g / mL,推荐的病毒混合比例为AAV-EF1α-DIO-GFP-TVA与AAV-EF1α-DIO-RVG按照体积比1:2混合。
2、推荐的注射体积为混合后的总体积100-300 nL,注射速度为20-50 nL/min。若目标核团较小或Cre在该区域的外周围也有较多表达,为控制起始感染区域的特异性,可适当降低注射AAV病毒的体积及速度;反之,如需标记大范围或Cre只在局部区域高特异性表达,可增加AAV注射的体积与速度。
3、为保证RV-EnvA-ΔG-dsRed注射时已有高丰度表达的TVA介导其感染神经元及G蛋白补偿其跨突触能力,AAV注射后需表达两周以上六周以内再注射RV-EnvA-ΔG-dsRed,六周以外未进行相关实验评估,但可尽量缩短AAV感染时间以缩短实验周期及避免AAV过表达外援TVA及G蛋白导致的细胞毒性及神经网络改变;RV注射后一般以一周为标准时间牺牲动物,而此时间也可控制在6-11天,对跨突触标记结果无太大影响(所有实验样本都需保证采用一致的时间窗口)。
|
病毒编号 |
病毒名称 |
病毒颜色及用途 |
|
R01001 |
RV-EnVA-△G-EGFP |
绿色,与AAV-RV(G)、AAV-TVA连用,可实现逆向跨单突触 |
|
R01002 |
RV-EnVA-△G-dsRed |
红色,与AAV-RV(G)、AAV-TVA连用,可实现逆向跨单突触 |
|
R01003 |
RV-EnVA-△G-Gcamp 6s-dsRed |
红色,与AAV-RV(G)、AAV-TVA连用,可实现逆向跨单突触;钙离子成像 |
|
R03001 |
RV-N2C(G)-△G-EGFP |
绿色,不跨突触,逆向高效标记 |
|
R03002 |
RV-N2C(G)-△G-dsRed |
红色,不跨突触,逆向高效标记 |
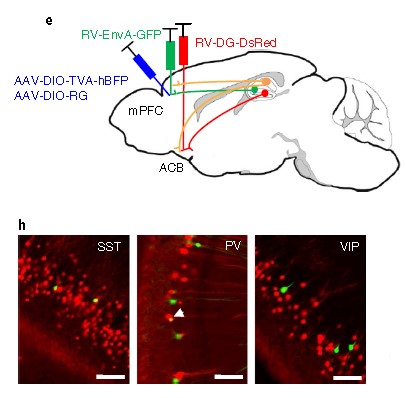
案例一:华中科技大学骆清铭课题组在抑制性神经元(SST, PV, VIP)的Cre小鼠mPFC脑区注射RV-EnvA-GFP以及Cre依赖的辅助病毒AAV-DIO-TVA-hBFP和AAV-DIO-RG实现逆向跨单级突触,同时在ACB脑区注射从轴突末梢吸收的RV-DG-DsRed,病毒逆向标记海马体投射到ACB区的神经元,最终找到海马体中同时调控mPFC和ACB区的GABA能神经元。(如图5)
图5 标记海马锥体神经元中同时作用于mPFC和ACB中的GABA能神经元(Sun et al.,Nature neuroscience, 2019)
案例二:暨南大学任超然课题组在Opn4-Cre小鼠LHb脑区注射RV病毒SAD-DG-DsRed (EnvA),在vLGN/IGL区注射表达TVA和RVG的AAV辅助病毒,实现逆向跨单级突触,发现m4型mRGCs直接激活vLGN/IGL-LHb通路。(如图6)
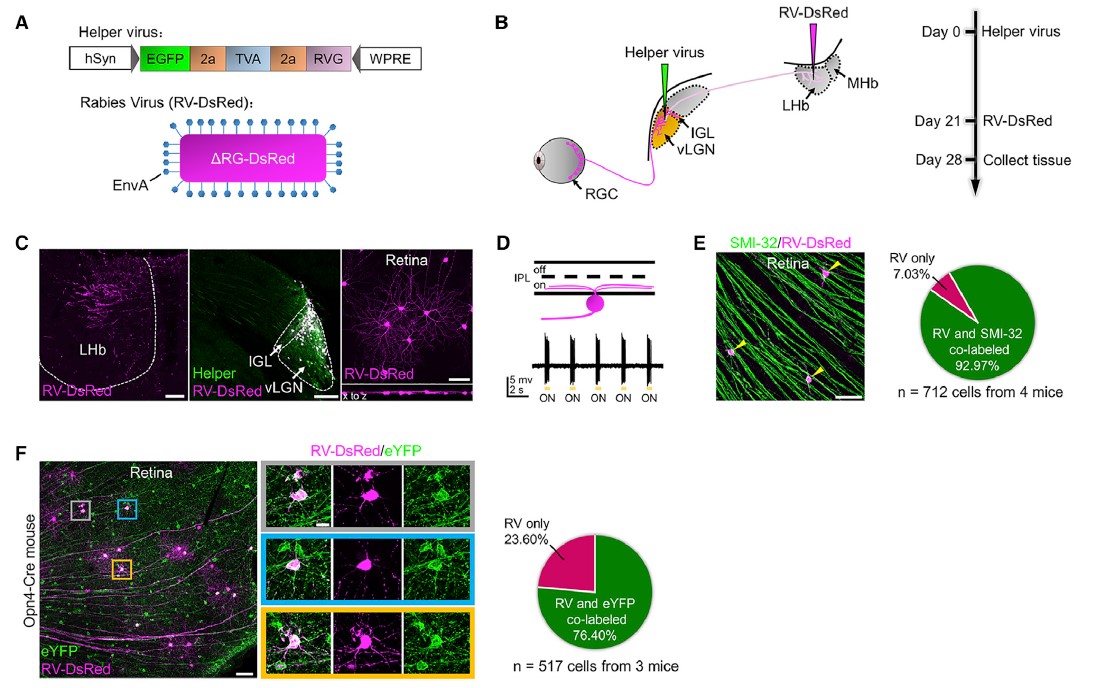
图6 m4型mRGCs直接激活vLGN/IGL-LHb通路(Huang et al.,Neuron, 2019)
1. Callaway, E.M., and Luo, L. (2015).Monosynaptic Circuit Tracing with Glycoprotein-Deleted Rabies Viruses.J Neurosci35, 8979-8985.
2. Sun, Q., Li, X., Ren, M., Zhao, M., Zhong, Q., Ren, Y., Luo, P., Ni, H., Zhang, X., Zhang, C., et al. (2019). A whole-brain map of long-range inputs to GABAergic interneurons in the mouse medial prefrontal cortex.Nature neuroscience.
3. Huang, L., Xi, Y., Peng, Y., Yang, Y., Huang, X., Fu, Y., Tao, Q., Xiao, J., Yuan, T., An, K., et al. (2019). A Visual Circuit Related to Habenula Underlies the Antidepressive Effects of Light Therapy.Neuron102, 128-142 e128.
信息订阅
我们将及时向您推送最新产品资讯

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com 客服:18140661572(活动咨询、售后反馈等)
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK